はじめに
私たちの生命活動にとってかけがえのない自然界に最も広く分布している色素群であるカロテノイド。その 600 種類を優に超えると言われている一群の中で、名が最もよく知られているカロテノイドは β-カロテンであることに異論を唱える人はいないでしょう。α-カロテンのページでも触れたように β-カロテンはプロビタミン A 活性の最も高いカロテノイドであることから、本ページでもビタミン A を抜きにして β-カロテンについて語ることはできません。
1913 年に McCollum らによって後にビタミン A と呼ばれるようになる因子の脂溶性 A(fat-soluble A)が彼らの動物実験で発見されて以来、α-カロテンページで列記したような欠乏症と共に、ビタミン A の重要性に対する認識が深まっていきました。1919 年頃までには、色が無いかまたは薄黄色の食物と黄色で主として植物に由来する食物の 2 種類に活性のあることがわかり始め、脂溶性ビタミンは黄色の植物性色素またはそれと関係する物質とみなすのが合理的に考えて安全であろうとする仮説が Steenbock によって立てられるようになりました。その有効成分がカロテンであることが確認されたのは 1928 年のことでした(Euler ら)。さらに、構造式が決定され(Karrer ら)、β-カロテンと α-カロテン、そして γ-カロテンといった種類のあることが見出されたのは 1930 年代に入ってからのことでした(Kuhn ら)[1-5]。
β-カロテンの主要な供給源:
カロテン(  carotene、
carotene、 carotène、
carotène、 Carotin )は元来ラテン語の carota にドイツ語の化学物質名に使われる接尾辞-in(e)を付して作り出され[6]、また、中国語でも
Carotin )は元来ラテン語の carota にドイツ語の化学物質名に使われる接尾辞-in(e)を付して作り出され[6]、また、中国語でも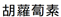 あるいは
あるいは と写し、文字通り「北方と西方の異民族より入った(=
と写し、文字通り「北方と西方の異民族より入った(=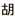 )ダイコン(=
)ダイコン(=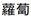 )」に見出される物質とされるように、洋の東西を問わず命名の由来となった植物はニンジン(学名:Daucus carota L.)でした。
)」に見出される物質とされるように、洋の東西を問わず命名の由来となった植物はニンジン(学名:Daucus carota L.)でした。
このような経緯から β-カロテンあるいはカロテンと言えばキャロット、ニンジンという印象を強く受けますが、他にはどのような食品にその供給源を求めることができるのでしょうか。
最新の日本食品標準成分表によると[7]、α-カロテン同様、海産物である海苔に β-カロテンが極めて豊富に含まれていることがわかります(図 1)。
| 図1. | β-カロテン含有量(μg/100 g 可食部)の多い食品 20 品目 | 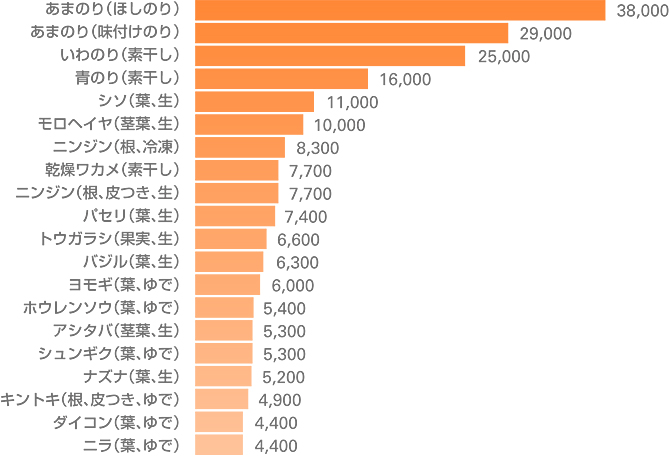 |
|
|
|||
このページでは β-カロテンに焦点を合わせていますが、食経験の長い海苔製品がさまざまな栄養素の宝庫であることは周知の事実です。
市販されている海苔は 1 枚 3 g 程度とされ、海苔だけで充分な栄養素を補おうにも限度があるかもしれませんが、野菜が苦手な人、日頃の食事から緑黄色野菜があまり取れていないと感じている人には、このような「海の野菜」の利用に工夫を凝らしてみるのも一案かも知れません。
また、陸の野菜でも、シソの葉や近年日本にも紹介され利用機会が増えつつあるモロヘイヤ(和名:シマツナソ;学名:Corchorus olitorius L.)(図 2)の茎・葉などにはニンジンを上回る量の β-カロテンが含まれていることがもう一つの興味深い点といえるでしょう。
| 図2. | モロヘイヤの葉(左)とモロヘイヤスープ(右) |  |
他、パセリやダイコンの葉も一般的な緑色葉菜より優れた β-カロテン供給源であり、前者であれば食することなしに料理の付け合せや飾りでおわらせたり、後者であれば切り落として捨てたりするのがいかにもったいないことであるかおわかり頂けるかと思います。

- 図3.
- みじん切りしたパセリをオリーブ油、レモン汁等で和えたタブーリの一例
例えば、アラビア料理の代表格とされるレバノン料理のサラダ(タブーリあるいはタブーレ、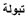 )にはみじん切りにしたパセリがふんだんに使われ(図 3)、また、ダイコンの葉もご存知のとおり古くより日本の家庭料理の中で多岐にわたって有効利用されてきたように、国内外の先人の知恵に学ぶことに限りはありません。
)にはみじん切りにしたパセリがふんだんに使われ(図 3)、また、ダイコンの葉もご存知のとおり古くより日本の家庭料理の中で多岐にわたって有効利用されてきたように、国内外の先人の知恵に学ぶことに限りはありません。
ビタミン A の最も重要な供給源としての β-カロテン:
厚生労働省が平成 21 年に発表した「日本人の食事摂取基準(2010 年版)」では、食品中のビタミン A 含量はレチノール当量として以下のような式で求められています[8]。
レチノール当量(μgRE)=レチノール(μg)+β-カロテン(μg)×1/12+α-カロテン(μg)×1/24+β-クリプトキサンチン(μg)×1/24+その他のプロビタミン A カロテノイド(μg)×1/24
プロビタミン A カロテノイドの変換率は β-カロテンが最も高いこと、また、ビタミン A 供給源がレバー、鶏卵、魚卵、ウナギのような魚類、酪農製品といった動物性食品よりも植物性食品に多く依存していることを考え合わせれば、食事性 β-カロテンがビタミン A 摂取量の変化に多大な影響を及ぼしていることがご理解頂けると思います。
しかしながら、同省が発表している平成 21 年国民健康・栄養調査の結果によりますと、ビタミン A の 1 日平均摂取量はレチノール当量(RE)で男性が 551 μg、女性が 522 μg とされ、男女ともに平成 20 年国民健康・栄養調査で発表のあった数値(それぞれ、626 μgRE、571 μgRE)と比べて減少し、日本人の食事摂取基準で推奨されている数値(成人男性で 800〜850 μgRE/日、成人女性で650〜700 μgRE/日)に到達するのが一層困難となっているのが現状です[8-10]
上述した摂取状況に加え、α-カロテンのページでも述べたように、ビタミン A は必須栄養素の一つとして欠かすことのできない成分であること、レチノールやレチノールエステルなどのビタミン A の形で過剰に摂取した場合にはリスクを生じる可能性はあるが、β-カロテンのようなプロビタミン A の形で高用量摂取してビタミン A の毒性が発現した例はみられないことから[11] ※ 、ビタミン A に関連した健康の維持・増進におけるプロビタミン A カロテノイドグループの有用性が益々重要視されることでしょう。
※ β-カロテン自体の安全性については後述します。
体内分布
β-カロテンは他のカロテノイド同様私たちの体内で合成されないため、日頃よりカロテノイドが豊富に含まれる食品から充分かつ適切な摂取を心掛けることが大切です。
食事に由来する β-カロテンをはじめとする複数のカロテノイドの存在が私たちの血液(表 1)や母乳中(母乳代替品である乳児用調整粉乳にも β-カロテンが配合されるようになりました)に認められます。現在までのところ 25 種類の食事性カロテノイドと 8 種 類 の カ ロ テ ノ イ ド 代 謝 物 ( そ れ ら の シ ス 異 性 体 は 除 く )が Khachik らの研究グループによって発見されています[12-14]。
- 表1.
- 野菜・果物を豊富に摂取している健常人の血清中の主要なカロテノイドの分布
| No. | 食事性カロテノイド | 血清中の分布(%) |
|---|---|---|
| 1 | ルテイン* | 20 |
| 2 | リコぺン* | 20 |
| 3 | β-カロテン* | 10 |
| 4 | α-カロテン* | 6 |
| 5 | ゼアキサンチン* | 3 |
| 6 | ζ-カロテン | 10 |
| 7 | フィトフルエン | 8 |
| 8 | β-クリプトキサンチン | 8 |
| 9 | α-クリプトキサンチン | 4 |
| 10 | フィトエン | 4 |
| 11 | アンハイドロルテイン | 3 |
| 12 | γ-カロテン | 2 |
| 13 | ニューロスポレン | 2 |
- * 発表時点(1997年)の商業的入手可能性を優先
- [文献 12 より引用改変]
Khachik ら(HPLC‐MS 分析)[13,15]、Hata ら(ラマン分光法、HPLC 分析)[16]の研究グループは、これまでにヒトの肝臓[15]、肺[15]、乳房[15]、子宮頚部[15]、皮膚[16]、大腸[13]、前立腺[13]といった組織から 1 gあたり ng から μg のレベルでカロテノイドとそれらの代謝物について過去に類をみない包括的な検出を行い、ヒトの血清中に存在が認められる食事性カロテノイドがこれらの器官や組織にも蓄積していることを明らかにしました(表 2)。
| 表2. | ヒトの組織と皮膚における食事性カロテノイドとそれらの代謝物 |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
カロテノイド豊富な食品の消費と癌や心血管疾患のような慢性疾患の発生低下を関連付けた近年の疫学調査は、この保護作用を広範囲のカロテノイド類の摂取量の高値によるものと考えましたが、時として一部の疫学調査では、このような保護作用に関与している可能性のあるカロテノイドを 1 種類あるいは 2 種類に絞ることができました。リコペンのページでみられる前立腺癌との関係、ルテインとゼアキサンチンのページでみられる AMD や加齢性白内障のような老化に伴ってリスクが上昇する眼疾患との関係などが例として挙げられます。
トマトあるいはトマトベースの食品の豊富な摂取と前立腺癌の発生低下との間で見出される強い相関は主としてそのような食品に存在するリコペンによるものとされていますが、トマトやトマト製品には γ-カロテン、ニューロスポレン、ζ-カロテン、フィトエン、フィトフルエンといった他の多くのカロテノイドが含まれており、これらがリコペンと共に前立腺を保護している可能性のあることも報告されています[17]。
また、AMD や加齢性白内障と密接なつながりのある網膜中心部や水晶体に特異的な蓄積が認められる食事性カロテノイドのルテイン・ゼアキサンチンがその局在部位で抗酸化剤としてのみならず光学フィルターとしても働いていることは、本サイトの当該ページで述べたとおりです。
しかしながら、ヒトの眼の他の組織に関する詳細な分析から[18]、例えば、網膜色素上皮(RPE:網膜の下に存在し、その下に脈絡膜、強膜が続く)や毛様体(図 4)には、これらの組織を酸化障害から同じように保護している可能性のある食事性カロテノイドが広範囲に存在することが明らかにされています(表 3)。
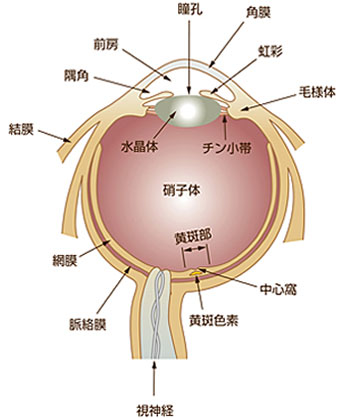
- 図4.
- ヒトの眼の構造(模式図)
網膜色素上皮の健全かつ適切な機能は同組織からルテインとゼアキサンチンを黄斑部に運搬するうえで重要な役割を果たしていると考えられることから、網膜色素上皮に存在する β-カロテンをはじめとするカロテノイドが AMD 予防に直接的に関与している可能性のあることが示唆されています。
以上のことから、疾病予防においてすべての食事性カロテノイドの有効性と集合な防護効果を評価する際、これらの化合物の混合物(マルチカロテノイド)による補給試験が論理的な取り組みの一つとなりそうです[19]。
長年にわたりさまざまな食事療法を受けたヒトの血清について広範囲の分析を行い、血清カロテノイドの相対濃度は食品に含まれるカロテノイドの比を(少なくともある程度まで)反映していることを明らかにした研究に携わってきたお一人の Khachik 博士は、カロテノイド豊富な野菜・果物の高摂取を癌のような慢性疾患の発生リスク減少と関連付けた疫学調査を解釈する際、この保護作用が β-カロテンのみに起因していると考えるべきではないと述べています[12-15]。
次章では、本ページの主題とも言える β-カロテンの光と影に焦点を合わせながら、これまでに発表された主要な研究について概観し、先に述べた事柄の真意をさらに理解できるよう試みたいと思います。
- 表3.
- ヒト毛様体、RPE-脈絡膜に含まれるルテイン・ゼアキサンチン以外の食事性カロテノイドの濃度
| カロテノイド濃度(ng/組織) | ||
|---|---|---|
| カロテノイドの種類 | 毛様体 | RPE-脈絡膜 |
| モノヒドロキシカロテノイド | ||
| α-クリプトキサンチン | 1.36 | N.D.* |
| β-クリプトキサンチン | 0.36 | N.D.* |
| 炭化水素カロテノイド | ||
| α-カロテン | 1.60 | 2.97 |
| β-カロテン | 2.72 | 10.80 |
| リコペン | 7.80 | 8.64 |
| γ-カロテン | 4.48 | N.D.* |
| ニューロスポレン | 4.50 | N.D.* |
| 合計 | 22.82 | 22.41 |
- * 検出せず
- [文献 18 より引用改変]
報告されている健康上の利点
最近のカロテノイド研究では、とりわけルテインやゼアキサンチンのようなキサントフィルカロテノイドと AMD のような加齢性眼疾患のリスクとの関係を調査した研究がさまざまな分野で散見され、カロテン類のみならずキサントフィル類にも多大な関心が寄せられるようになりました。全米 5 ヵ所の眼科施設においてカロテノイド、ビタミン A、E、C の食事摂取と AMD リスクの関係を評価した多施設症例対照研究で、食事性ルテイン・ゼアキサンチン摂取量の最低五分位群(同約 0.6 mg)と比較した最高五分位群(1 日約 5.8 mg)における 57%の統計上有意(p<0.001)な AMD のリスク低下に加え、カロテノイド摂取量や β-カロテン摂取量についても有意な低下(それぞれ 43% (p=0.02)、41% (p=0.03))が認められていたことをおぼえていらっしゃるでしょうか[20]。
β-カロテン研究は冒頭で述べた 1900 年代初期にプロビタミン A としての働きに注目されて以来の長い歴史があり、さらにその抗酸化剤としての働きと共に検討される分野も多岐に渡りました。ここでは、その中で最も重要とされる分野の一つとして、肺癌をはじめとする何種類かの癌のハイリスクグループを対象とした研究を中心に述べていきたいと思います。
癌のリスクに関する観察的研究から
β-カロテン、カロテン類、カロテノイド類の血中濃度、あるいはそれらを豊富に含む野菜・果物のような食品の消費と慢性疾患の一つである癌のリスクとの関連性を評価した疫学的な研究は 1992 年までに発表された観察的研究に限定しても数多く存在し(表 4、5)[21]、さらに β-カロテンあるいは β-カロテンと他の考え得る栄養素との組合せの摂取が一定の癌の予防に果たす推定上の役割により多くの洞察をもたらそうとする大規模介入試験の結果も発表されることになります[22-25]。
表4. 食事性カロテノイド摂取と部位別の癌に関する後向き研究(1977 年〜1992 年)
| 部位 | 著者 | 発表年 | 症例数 | 曝露評価 | 関連性 | 相対危険度 | 母集団 | |
|---|---|---|---|---|---|---|---|---|
| 肺 | MacLennan ら | 1977 | 233 | 緑色野菜インデックス | ↓ | 0.45 | 男女、中華系、シンガポール | |
| Kolonel ら | 1983 | 267 | カロテノイド | ↓ | 0.40 | 男女、多民族、ハワイ州 | ||
| Hinds ら | 1984 | 364 | カロテノイド | ↓ | 0.45 | 男女、多民族、ハワイ州 | ||
| Wu ら | 1985 | 216 | β-カロテン | ↓ | 0.40 | 女性、白人、ロスアンゼルス郡 | ||
| Samet ら | 1985 | 447 | カロテノイド | n.s. | 0.76 | 男女、白人、ニューメキシコ州 | ||
| Ziegler ら | 1986 | 763 | カロテノイド | ↓ | 0.59 | 男性、白人、ニュージャージー州 | ||
| Pisani ら | 1986 | 417 | ニンジン、緑色野菜 | ↓ | 0.50 | 男女、北イタリア | ||
| Bond ら | 1987 | 308 | カロテノイド | n.s. | 0.42 | 化学会社従業員、テキサス州 | ||
| Byers ら | 1987 | 450 | カロテノイド | ↓ | 0.63 | 男女、ニューヨーク州 | ||
| Pastorino ら | 1987 | 47 | カロテノイド | n.s. | 0.34 | 女性、北イタリア | ||
| Koo ら | 1988 | 88 | カロテノイド豊富野菜 | n.s. | 0.60 | 女性、中国人、香港 | ||
| Fontham ら | 1988 | 1,253 | カロテノイド | n.s. | 0.88 | 男女、ルイジアナ州南部 | ||
| Le Marchand ら | 1989 | 332 | β-カロテン | ↓ | 0.53 | 男女、多民族、ハワイ州 | ||
| Jain ら | 1990 | 839 | β-カロテン | n.s. | 0.89 | 男女、トロント地区 | ||
| Dartiques ら | 1990 | 106 | カロテノイド | ↓ | 0.25 | 男女、フランス南西部 | ||
| Harris ら | 1991 | 96 | カロテノイド | ↓ | 0.45 | 男性、英国 | ||
| Wu-Williams ら | 1991 | 965 | カロテノイド豊富野菜 | n.s. | 0.90 | 女性、中国東北地方 | ||
| 食道 | Ziegler ら | 1981 | 120 | カロテン | n.s. | 0.77 | 男性、黒人、ワシントン DC | |
| Tuyns ら | 1987 | 743 | カロテン | ↓ | 0.47 | 男女、フランス、カルバドス県 | ||
| Decarli ら | 1987 | 105 | β-カロテン | ↓ | 0.23 | 男女、北イタリア | ||
| Brown ら | 1988 | 209 | カロテン | n.s. | 0.80 | 男性、サウスカロライナ州 | ||
| Graham ら | 1990 | 178 | カロテン | n.s. | 0.66 | 男女、ニューヨーク州 | ||
| 口腔 | Winn ら | 1984 | 227 | 野菜・果物 | ↓ | 0.5 | 女性、黒人、白人、米国南部 | |
| 咽頭 | McLaughin | 1988 | 871 | カロテン | n.s. | 0.9;0.8f | 男女、白人、米国 | |
| Rossing | 1989 | 166 | カロテノイド | n.s. | 1.0 | 男女、ワシントン州 | ||
| Ning ら | 1990 | 100 | ニンジン | n.s. | 0.4 | 男女、天津、中国 | ||
| 胃 | Correa ら | 1985 | 391 | カロテノイド | n.s. | 0.68;1.08 | 男女、ルイジアナ州(白人;黒人) | |
| Risch ら | 1985 | 246 | β-カロテン | ↓ | 0.33 | 男女、カナダ | ||
| Jedrichowski | 1986 | 110 | 野菜・果物 | ↓ | 0.24 | 男女、クラクフ、ポーランド | ||
| La Vechia | 1987 | 206 | β-カロテン | ↓ | 0.39 | 男女、北イタリア | ||
| You ら | 1988 | 564 | カロテン | ↓ | 0.50 | 男女、山東省農村部、中国 | ||
| 膵臓 | Gold ら | 1985 | 201 | 野菜・果物(生) | ↓ | 0.55 | 男女、ボルティモア地区 | |
| Norell ら | 1986 | 99 | 野菜 | n.s. | 0.5 | 男女、スウェーデン | ||
| Falk ら | 1988 | 363 | カロテノイド | n.s. | 0.82m;1.65f | 男女、ルイジアナ州 | ||
| Olsen ら | 1989 | 212 | 野菜 | n.s. | 0.95 | 男性、白人、ミネアポリス地区 | ||
| 結腸、直腸 | Macquart-Moulin ら | 1986 | 399 | 野菜 | ↓ | 0.42m;0.68f | 男女、マルセイユ地区 | |
| Potter ら | 1986 | 419 | β-カロテン | n.s. | 0.8m;2.2f | 男女、南オーストラリア州 | ||
| Kune ら | 1987 | 715 | β-カロテン | ↓ | 0.45 | 男女、メルボルン | ||
| Graham ら | 1988 | 428 | カロテン | n.s. | ― | 男女、ニューヨーク州 | ||
| La Vecchia ら | 1988 | 575 | 緑色野菜 | ↓ | 0.5 | 男女、北イタリア | ||
| West ら | 1989 | 231 | β-カロテン | ↓ | 0.4m;0.6f | 男女、ユタ州 | ||
| Freudenheim ら | 1990 | 423 | カロテノイド | ↓ | 0.59m;0.70f | 男女、ニューヨーク州 | ||
| Peters ら | 1989 | 147 | 野菜・果物(生) | ↓ | 0.59 | 男女、ロサンゼルス郡 | ||
| Young ら | 1988 | 353 | 黄色野菜 | n.s. | 0.78 | 男女、白人、ウィスコンシン州 | ||
| Slattery ら | 1988 | 231 | 野菜 | n.s. | 0.6 | 男女、白人、ユタ州 | ||
| Bidoli ら | 1992 | 148 | 野菜 | n.s. | 0.6 | 男女、北イタリア | ||
| 膀胱 | Dunham ら | 1968 | 493 | 葉菜、黄色野菜 | n.s. | ― | 男女、黒人、白人、ルイジアナ州 | |
| Mettlin ら | 1979 | 569 | ニンジン | ↓ | 0.62 | 男女、ニューヨーク州 | ||
| La Vecchia ら | 1989 | 163 | カロテノイド | ↓ | 0.41 | 男女、北イタリア | ||
| Risch ら | 1988 | 826 | β-カロテン | n.s. | 0.95 | 男女、カナダ | ||
| Claude ら | 1986 | 431 | 野菜・果物 | ↓m | 0.59m;0.90f | 男女、北ドイツ | ||
| 子宮頚管 | Marshall ら | 1983 | 513 | β-カロテン | ↓ | 0.50 | 女性、白人、ニューヨーク州 | |
| Brock ら | 1988 | 117 | β-カロテン | ↓ | 0.5 | 女性、シドニー、オーストラリア | ||
| La Vecchia ら | 1988 | 392 | β-カロテン | n.s. | 0.18;1.09 | 女性、北イタリア(浸潤性;上皮内) | ||
| Verreault ら | 1989 | 189 | カロテノイド | n.s. | 0.6 | 女性、ワシントン州 | ||
| Ziegler ら | 1990 | 271 | カロテノイド | n.s. | 0.98 | 女性、白人、米国 | ||
| van Eenwijk ら | 1991 | 102 | β-カロテン | n.s. | 0.56 | 女性、シカゴ、米国 | ||
| 乳房 | La Vecchia ら | 1987 | 1,108 | 緑色野菜 | ↓ | 0.42 | 女性、北イタリア | |
| Iscovich ら | 1989 | 150 | β-カロテン | n.s. | 0.92 | 女性、アルゼンチン | ||
| Katsouyanni ら | 1988 | 120 | カロテン | ↓ | 0.56 | 女性、ギリシア | ||
| Rohan ら | 1988 | 451 | β-カロテン | ↓ | 0.76 | 女性、南オーストラリア州 | ||
| Marubini ら | 1988 | 214 | β-カロテン | n.s. | 1.20 | 女性、北イタリア | ||
| Toniolo ら | 1989 | 250 | β-カロテン | n.s. | 1.00 | 女性、北イタリア | ||
| van't Veer ら | 1990 | 133 | β-カロテン | n.s. | 0.73 | 女性、オランダ | ||
| Potischman ら | 1990 | 83 | カロテノイド | n.s. | 0.81 | 女性、ニューヨーク州 | ||
| Richardson ら | 1991 | 409 | β-カロテン | n.s. | 1.0 | 女性、モンペリエ、フランス | ||
| 卵巣 | Slattery ら | 1989 | 85 | β-カロテン | ↓ | 0.50 | 女性、白人、米国 | |
| Byers ら | 1983 | 274 | カロテノイド | n.s. | 0.77 | 女性、ニューヨーク州 | ||
| La Vecchia ら | 1987 | 455 | カロテン | n.s. | 0.94 | 女性、北イタリア | ||
| Shu ら | 1989 | 172 | カロテン | n.s. | 1.0 | 女性、上海、中国 | ||
| 前立腺 | Ohno ら | 1988 | 100 | β-カロテン | ↓ | 0.34 | 男性、日本 | |
| Ross ら | 1987 | 142 | β-カロテン | n.s. | 0.6;1.0 | 男性、カリフォルニア州(黒人;白人) | ||
| Mishina ら | 1985 | 100 | 緑黄色野菜 | n.s. | 0.5 | 男性、日本 | ||
| Talamini ら | 1986 | 166 | 緑色野菜 | n.s. | 1.20 | 男性、ポルデノーネ 、イタリア | ||
| Mettlin ら | 1989 | 371 | β-カロテン | ↓ | 0.60 | 男性、ニューヨーク州 | ||
| Oishi ら | 1988 | 100 | β-カロテン | ↓ | 0.47 | 男性、日本 | ||
| Le Marchand ら | 1991 | 452 | β-カロテン | n.s. | ― | 男性、多民族、ハワイ州 | ||
| n.s.:統計学的有意差を認めず、↓:統計学的に有意な逆相関関係を認める、f:女性についのみのデータ、m:男性についてのみのデータ | ||||||||
| [文献 21 より引用改変] | ||||||||
表5. 食事性カロテノイドの摂取量あるいは血中濃度と部位別の癌に関する前向き研究(1979 年〜1991 年)
| 部位 | 著者 | 発表年 | 症例数 | 曝露評価 | 関連性 | 相対危険度 | 母集団 | |
|---|---|---|---|---|---|---|---|---|
| 肺 | Shekelle ら | 1981 | 33 | カロテノイド摂取量 | ↓ | 0.14 | 男性、Western Electric Study | |
| Willett ら | 1984 | 17 | 血漿総カロテン濃度 | n.s. | ― | 男女、米国 | ||
| Nomura ら | 1985 | 74 | 血漿 β-カロテン濃度 | ↓ | 0.29 | 男性、日系人、ハワイ州 | ||
| Long-de ら | 1985 | 2,952 | グリーンサラダ、果物 | ↓ | 0.56 | 男女、中国 | ||
| Hirayama ら | 1986 | 1,917 | 緑黄色野菜 | ↓ | 0.79m;1.35f | 男女、日本 | ||
| Kromhout ら | 1987 | 63 | カロテノイド摂取量 | n.s. | 0.68 | 男女、ジュトフェン、オランダ | ||
| Paganini-Hill ら | 1987 | 56 | カロテノイド摂取量 | n.s. | 0.72m;0.67f | 男女、Leisure World、ロサンゼルス | ||
| Wald ら | 1988 | 50 | 血漿 β-カロテン濃度 | ↓ | 0.41 | 男性、BUPA Study、英国 | ||
| Connett ら | 1989 | 66 | 血漿 β-カロテン濃度 | ↓ | 0.43 | 男性、MRFIT Study、米国 | ||
| Knekt ら | 1990 | 108 | 血漿 β-カロテン濃度 | n.s. | 1.00 | 男女、フィンランド | ||
| Knekt ら | 1991 | 108 | カロテノイド摂取量 | ↓ | 0.40;0.93 | 男性、フィンランド(非喫煙者;喫煙者) | ||
| Fraser ら | 1991 | 61 | 果物、グリーンサラダ | ↓ | 0.26;0.65 | 男女、白人、California Adventists(果物;サラダ) | ||
| Stähelin ら | 1991 | 64 | 血漿総カロテン濃度 | ↓ | 0.56 | 男女、Basel Study | ||
| Comstock ら | 1991 | 99 | 血漿 β-カロテン濃度 | ↓ | 0.45 | 男女、ワシントン郡 | ||
| Orentreich ら | 1991 | 123 | 血漿 β-カロテン濃度 | ↓ | 0.33 | 男女、米国 | ||
| 胃 | Nomura ら | 1985 | 70 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、日系人、ハワイ州 | |
| Hirayama ら | 1986 | 5,247 | 緑黄色野菜 | ↓ | 0.66m;0.66f | 男女、日本 | ||
| Wald ら | 1988 | 13 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、BUPA Study、英国 | ||
| Knekt ら | 1990 | 32 | 血漿 β-カロテン濃度 | n.s. | 0.8 | 男女、フィンランド | ||
| Stähelin ら | 1991 | 16 | 血漿総カロテン濃度 | ↓ | 0.34 | 男女、Basel Study | ||
| 膵臓 | Mills ら | 1988 | 40 | 緑色野菜、グリーンサラダ | n.s. | ― | 男女、California Adventists | |
| Knekt ら | 1990 | 10 | 血漿 β-カロテン濃度 | n.s. | 0.60 | 男女、フィンランド | ||
| Comstock ら | 1991 | 22 | 血漿 β-カロテン濃度 | n.s. | 0.83 | 男女、ワシントン郡 | ||
| 結腸、直腸 | Shekelle ら | 1981 | 49 | 食事性カロテノイド | n.s. | ― | 男性、Western Electric Study | |
| Nomura ら | 1985 | 113 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、日系人、ハワイ州 | ||
| Paganini-Hill ら | 1987 | 110 | 食事性カロテノイド | n.s. | 0.90m;1.17f | 男女、Leisure World、ロサンゼルス | ||
| Schber ら | 1987 | 72 | 血漿 β-カロテン濃度 | n.s. | 0.83 | 男女、白人、ワシントン郡 | ||
| Wald ら | 1988 | 30 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、BUPA Study、英国 | ||
| Heilbrun ら | 1989 | 162 | 食事性 β-カロテン | n.s. | 0.72 | 男性、日系人、ハワイ州 | ||
| Connett ら | 1989 | 14 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、MRFIT Study、米国 | ||
| Knekt ら | 1990 | 13 | 血漿 β-カロテン濃度 | n.s. | 0.30 | 男女、フィンランド | ||
| Comstock ら | 1991 | 106 | 血漿 β-カロテン濃度 | n.s. | 0.83;1.25 | 男女、ワシントン郡(結腸;直腸) | ||
| Stähelin ら | 1991 | 32 | 血漿総カロテン濃度 | n.s. | 0.76 | 男女、Basel Study | ||
| 膀胱 | Shekelle ら | 1981 | 19 | 食事性カロテノイド | n.s. | ― | 男性、Western Electric Study | |
| Nomura ら | 1985 | 27 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、日系人、ハワイ州 | ||
| Paganini-Hill ら | 1987 | 59 | 食事性カロテノイド | ↓ | 0.62m;0.15f | 男女、Leisure World、ロサンゼルス | ||
| Wald ら | 1988 | 15 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、BUPA Study、英国 | ||
| Knekt ら | 1990 | 18 | 血漿 β-カロテン濃度 | n.s. | 0.30 | 男女、フィンランド | ||
| Comstock ら | 1991 | 35 | 血漿 β-カロテン濃度 | n.s. | 0.63 | 男女、ワシントン郡 | ||
| 乳房 | Hirayama ら | 1979 | 142 | 緑黄色野菜 | n.s. | ― | 女性、日本 | |
| Wald ら | 1984 | 39 | 血漿 β-カロテン濃度 | n.s. | 0.35 | 女性、ガーンジー、英国 | ||
| Willett ら | 1984 | 14 | 血漿総カロテン濃度 | n.s. | ― | 女性、高血圧症フォローアップ、米国 | ||
| Paganini-Hill ら | 1987 | 123 | 食事性カロテノイド | n.s. | 0.83 | 男女、Leisure World、ロサンゼルス | ||
| Comstock ら | 1991 | 30 | 血漿 β-カロテン濃度 | n.s. | 0.9 | 女性、閉経後、ワシントン郡 | ||
| 前立腺 | Shekelle ら | 1981 | 29 | 食事性カロテノイド | n.s. | ― | 男性、Western Electric Study | |
| Willett ら | 1984 | 11 | 血漿総カロテン濃度 | n.s. | ― | 男性、高血圧症フォローアップ、米国 | ||
| Snowdown ら | 1984 | 247 | 野菜・果物 | n.s. | ― | 男性、Seventh Day Adventists | ||
| Hirayama ら | 1986 | 183 | 緑黄色野菜 | n.s. | 1.23 | 男性、日本 | ||
| Paganini-Hill ら | 1987 | 93 | 食事性カロテノイド | n.s. | ― | 男女、Leisure World、ロサンゼルス | ||
| Mills ら | 1988 | 180 | 野菜・果物 | ↓ | 0.70;0.68 | 男性、California Adventists(果物;サラダ) | ||
| Knekt ら | 1990 | 32 | 血漿 β-カロテン濃度 | ↓. | 0.20 | 男女、フィンランド | ||
| Comstock ら | 1991 | 103 | 血漿 β-カロテン濃度 | n.s. | 0.91 | 男性、ワシントン郡 | ||
| 皮膚 | Shekelle ら | 1981 | 36 | 食事性カロテノイド | n.s. | ― | 男性、Western Electric Study、米国 | |
| Wald ら | 1988 | 56 | 血漿 β-カロテン濃度 | n.s. | ― | 男性、BUPA Study、英国 | ||
| Knekt ら | 1991 | 38 | 血漿 β-カロテン濃度 | n.s. | 0.32 | 男女、フィンランド | ||
| n.s.:統計学的有意差を認めず、↓:統計学的に有意な逆相関関係を認める、f:女性についのみのデータ、m:男性についてのみのデータ | ||||||||
| [文献 21 より引用改変] | ||||||||
これらの疫学研究で得られた結果を解釈する際、食事摂取あるいは血中濃度の調査では関連性が特定のカロテノイドによるものであるかは決定できないこと、食事摂取の評価の粗さによる誤分類は関連性を減弱するおそれがあること、前向き研究では被験者における想起の偏り(recall bias)に見舞われる可能性があることなどのような点に留意する必要がありますが、後向き研究の結果からカロテノイド豊富な野菜・果物の高摂取が多くの部位における癌のリスク低下と関連のあることが明らかにされています(表 4)。さらに、この関連性は肺と胃の癌で最も整合性が高く、逆に乳房、前立腺、食道、口腔の癌で低いように思われます。
前向き研究では、カロテノイドの逆の関係は肺癌と著しい一貫性が認められます(表 5)。胃癌に関して前向き研究で得られたエビデンスも類似していますが、それらの研究の強度と数は中等度のようです。乳癌と前立腺癌については、後向き研究で得られた結果と一致を見せていますが、血漿カロテンあるいは食事性カロテンとリスク低下との一貫した関連は明らかではありません。また、他の部位の癌については、両研究とも症例数がしばしば少なくなり、強い関連性は前向き研究でのみ検出される可能性が示唆されます[21]
癌のリスクに関する介入試験から
前項で列挙した多数の観察的研究から得られた有望な結果を受け、特定の人口集団を対象とした複数の大規模な介入試験が実施されました。
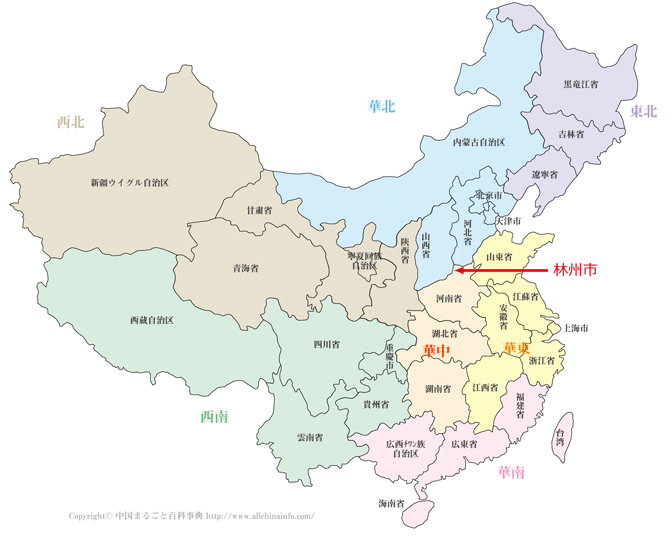
1980 年代半ばに米国国立癌研究所が野菜・果物における食事摂取の補助として β-カロテンと他のビタミン・ミネラルの化学予防に関して計画した試験のうちの著名なものとして、1986 年から 1991 年まで中国河南省の (Linxian リンシャン:現在の林州市、図 5)で実施された一対の試験があります[22,23]。
(Linxian リンシャン:現在の林州市、図 5)で実施された一対の試験があります[22,23]。
| 図5. | 中国における (現在の林州市)の (現在の林州市)の所在地 |
 |
研究者は、食道/胃噴門癌の発生率が世界で最も高い集団の一つであり(同癌による死亡率は中国国内平均の 10 倍、米国における白人の 100 倍を超える)、何種類かの微量栄養素の摂取量が遺存的に少ないとされるリンシャンの住民を対象に、特定の食事性ビタミン・ミネラルの補給が同母集団における癌の発生率、癌による死亡率、あるいは他の疾病による死亡率を低下するかについて調査を行いました[22]。
40 歳から 69 歳までの参加者は、(A)レチノールと亜鉛、(B)リボフラビンとナイアシン、(C)ビタミン C とモリブデン、そして(D)β-カロテン、ビタミン E、セレニウムいずれかの組合せの投与を受けるために無作為に割り付けられました(表 6)。
表6. 各群に投与される微量栄養素の種類と用量
| 投与群 | 微量栄養素 | 1 日用量 |
|---|---|---|
| A | レチノール(パルミチン酸塩として) | 5,000 IU |
| 亜鉛(酸化亜鉛として) | 22.5 mg | |
| B | リボフラビン | 3.2 mg |
| ナイアシン | 40 mg | |
| C | アスコルビン酸 | 120 mg |
| モリブデン(モリブデン酵母複合体として) | 30 μg | |
| D | β-カロテン | 15 mg |
| セレニウム(セレニウム酵母として) | 50 μg | |
| α-トコフェロール | 30 mg | |
| [文献 22 より引用改変] | ||
5 年間の試験の終了時、これらの組合せのうちで食道癌あるいは胃癌の発生を見事に減少させたものはありませんでしたが、その中でも D の β-カロテン、ビタミン E、セレニウムの組合せの投与を受けた群が健闘し、全癌死亡における相対危険度(RR)は 0.87[95%信頼区間 (CI): 0.75〜1.00]、全死亡における RR は 0.91[95% CI: 0.84〜0.99]、食道癌による死亡における RR は 0.96[95% CI: 0.78〜1.18]、さらに胃癌による死亡における RR は 0.79[95% CI: 0.64〜0.99]という著しいリスク低下が認められました。
同研究論文あるいは他の関連するレビュー論文でコメントされているように、今回得られた結果は確定的でないものの、このような前途有望な所見がβ-カロテンをはじめとする微量栄養素の補給がもたらし得る健康上の有益性を明確化するための研究を促すきっかけになったのかもしれません。
さらに、1998 年の Epidemiology に発表された論説では[23]、リンシャンの母集団の均一的な民族性と初期栄養欠乏状態を考慮すれば、これらの研究で対象となった母集団から得られた所見を標準的な米国人あるいは西洋の母集団と関連付けることは困難である一方、この母集団が癌や動脈硬化性疾患の発生率上昇と関係する西洋型リスクファクターが発現しつつある第三世界における多数の人々の代表となっているとされ、癌や血管疾患の予防における野菜・果物中のキー栄養素についての疑問に答えようとする試みは国内外の研究において優先されるべき事柄であると述べられています。
リンシャンに居住する 40 歳から 69 歳までの男女 29,584 人を対象に行われたこの試験は、β-カロテン(の組合せ)補給についてポジティブな健康利益を実証した唯一の大規模化介入試験となってしまいました。
リンシャンの 3,318 人の住人を対象としたより小規模な二回目の試験では、食道癌の高リスクにある参加者が 15 mg の β-カロテンを含有するカプセルに加え、26 種類のビタミン・ミネラル(含む、葉酸、ビタミン B6、B12)を含有するカプセルの投与を受けました。6 年後、対応する群における食道癌プラス胃噴門癌による死亡の相対危険度(RR)は 0.92(95% CI: 0.62〜1.28)、食道癌による死亡の RR は0.84(95% CI: 0.54〜1.29)、全死亡の RR は 0.93(95% CI: 0.75〜1.16)、癌死亡の RR は 0.96(95% CI: 0.71〜1.29)と顕著な有益性が認められなかったばかりでなく、初回の試験で死亡リスクの著しい低下をみせた胃癌では死亡率の上昇も認められました(RR: 1.18、95% CI: 0.76〜1.85)。
このような当初の予想に反する結果は、リンシャンの住民のような栄養欠乏状態のみられない人口集団を対象とした Alpha-Tocopherol/Beta-Carotene (ATBC) Trial [24]、Beta-Carotene and Retinol Efficacy Trial (CARET) [25,26]、Physicians Health Study (PHS) [27] といったフィンランドや米国でほぼ同時期に実施された一連の大規模介入試験においても、同様にあるいはそれ以上に裏付けられ、私たちは言わば β-カロテン神話の崩壊という重大な局面を迎えることになります(表 7)
※ ここでは、肺癌のような癌のリスク以外、例えば心血管系の疾病リスクとの関係については取り上げていませんが、一部の研究の概要は文献データ ベースのページの「カロテノイド研究」でご覧いただけます。
表7. 微量栄養素の補給が癌予防に及ぼす影響を評価したフィンランドと米国における大規模介入試験の概略
| The Alpha-Tocopherol, Beta-Carotene Cancer Prevention (ATBC) Study | The Beta-Carotene and Retinol Efficacy Trial (CARET) | The Physicians' Health Study(PHS) | |
|---|---|---|---|
| 発表 | The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. The Alpha-Tocophenol, Beta Carotene Cancer Prevention Study Group. New England Journal of Medicine 1994; 330:1029-35. | Omenn GS, Goodman GE, Thornquist MD, Balmes J, Cullen MR, Glass A, Keogh JP, Meyskens FL Jr, Valanis B, Williams JH Jr, Barnhart S, Cherniack MG, Brodkin CA, Hammar S. Risk factors for lung cancer and for intervention effects in CARET, the Beta-Carotene and Retinol Efficacy Trial. J Natl Cancer Inst. 1996 Nov 6;88(21):1550-9. | Hennekens CH, Cook NR, et al. Lack of effect of long-term supplementation with beta carotene on the incidence of malignant neoplasms and cardiovascular disease. N Engl J Med 1996;334:1145-9. |
| 設計 | 無作為化二重盲検プラセボ対照比較試験 | 多施設無作為化二重盲検プラセボ対照比較試験 | 無作為化二重盲検プラセボ対照比較試験 |
| 実施機関 | 米国立癌研究所(NCI)、the National Public Health Institute of Finland | Fred Hutchinson Cancer Research Center, University of Washington School of Public Health, Seattle, Washington, USA | Division of Preventive Medicine, Department of Medicine, Brigham and Women's and Harvard Medical School, Boston, Massachusetts, USA |
| 試験期間 | 1985〜1993 年:フィンランド南西部 | 1985〜1996 年(予定を繰り上げて中止):試験は最終的にシアトル、ポートランド、バルチモア、サンフランシスコ、バルチモア、アービンの計 6 施設で 10 倍に拡大* | 1982 年〜1995 年 10 月 |
| 対象者 | 50〜69 歳、男性、喫煙者(タバコ 1 日 1 箱以上)、29,133 人 | 45〜74 歳、女性&男性、喫煙者、過去喫煙者、アスベストに曝された労働者、18,314 人 | 40〜84 歳、男性米国人医師(試験開始時点で喫煙者:11%、過去喫煙者:39%)、22,071 人 |
| 投与計画 | β-カロテン(20 mg/日)、ビタミン E(α-トコフェロールとして 50 mg/日)、β-カロテン+ビタミン E、orプラセボ | β-カロテン(30 mg/日)+ビタミン A(パルミチン酸レチノールとして 25,000 IU/日)、or プラセボ | β-カロテン(50 mg 隔日), or プラセボ |
| 目的 | 一定のビタミン補充が肺癌及び他の癌の一次予防に及ぼす影響の評価 | 高リスク母集団における肺癌の発生率に及ぼす影響の評価 | 癌の一次予防に及ぼす β-カロテンの影響を評価+ |
| 結果(一部) | [ビタミン E(α-トコフェロール)群] 肺癌の発生率低下は観察されなかった 全死亡率に及ぼす明らかな影響は認められなかった [β-カロテン群] 肺癌の発生率が 18%上昇した 肺癌以外の癌の発生率に及す影響は、ほとんどあるいは全く認められなかった 全死亡率は 8%上昇した 主に肺癌と虚血性心疾患に原因する死亡が多かった β-カロテン+ビタミン E についても同様の結果 |
[CARET 試験期間中] β-カロテン+ビタミン A 摂取群: 肺癌の発生率が 28%上昇した 全死亡率が 17%上昇した この結果により、試験は 21 ヵ月早く(1996 年 1月に)中止となった* [CARET 終了後の 6 年間の追跡調査** ] β-カロテン+ビタミン A 摂取群: 追跡期間中肺癌の発生リスクが 12%上昇した 全死亡率が 8%上昇した |
[N Engl J Med 1996] β-カロテン摂取群において、癌あるいは全死亡のリスクに及ぼす統計上有意な影響は認められなかった [Cancer 1999 ++] 12 年の追跡調査期間に癌と診断された 1,439 例(うち、631 例が前立腺癌)を対象 β-カロテン摂取群において、癌のリスクに及ぼす統計上有意な影響は認められなかった 投与前の血漿 β-カロテン濃度が最低の群では、前立腺癌のリスク低下の可能性が認められた |
| 結論 | α-トコフェロールあるいは β-カロテンの補給は実際に有益な作用ばかりでなく有害な作用も及ぼす可能性が提起される。 | 試験参加者で認められた肺癌リスクの持続的な上昇は、β-カロテンが引き起こす細胞の変化に原因している可能性がある**。 ** http://cancer.gov/clinicaltrials/results/final-CARET1204 |
++ ベースライン(もともと)の血中濃度が低い集団では、β-カロテンの補充が前立腺癌のリスクを低下させる可能性が示唆された。 同母集団におけるさらなる追跡調査が必要とされる。 |
| 備考 | 追跡期間:5〜8 年間 | 追跡期間:平均 6 年間 * J Natl Cancer Inst 1996; 88:1550-9 |
追跡期間:平均 12 年間、+ アスピリンが心血管疾患による死亡に及ぼす影響についてはここでは記載せず |
平均追跡期間が約 12 年と最長であった PHS では、β-カロテン 50 mg の隔日投与(=25 mg/日)に有益性を裏付ける証拠を得ることはできませんでした。ATBC と CARET の結果は、共に β-カロテンを含む微量栄養素の投与群で肺癌並びに全死亡率の上昇を認め、CARET ではその結果を受け予定より 21 ヵ月早い試験の中止に至り、β-カロテンの有効性と安全性についてこれまで考えられてきた殆どのことを劇的に変貌させました。このような混乱によって β-カロテンの用量や供給源に関する議論も際立つようになり、2000 年には欧州委員会の食品科学委員会[欧州安全機関(EFSA)の前身]による全ての供給源の β-カロテンの使用における安全性について意見書が提出されました[28]。
上述した欧州委員会の食品科学委員会をはじめとする主要な団体で発表されている β-カロテンの安全性に対する公式見解をまとめると下表のようになります。
表8. β-カロテンの安全値の比較
| CRN USA:米国栄養評議会 | サプリメントとしての上限摂取量 (ULS)[OSL 法] |
・非喫煙者について 25 mg/日 ・喫煙者は補給すべきでない |
The Physicians' Health Study の結果に基づいて、非喫煙者に対する OSL(観察された安全量)として 1 日摂取量を 25 mg に設定した。 |
| US FNB: 食品・栄養評議会(米国) |
許容上限摂取量(UL) | ・検討されたが設定されていない ・喫煙者は使用すべきでない |
β-カロテンに喫煙者の肺癌リスクを増大させる可能性を認めるが、データは UL を導くほどには十分でない。 |
| EC SCF: 欧州委員会の食品科学委員会 |
許容上限摂取量(UL) | ・検討されたが設定されていない ・喫煙者にはリスクを伴う |
喫煙者への 20 mg/日の β-カロテン補給にリスク増大の可能性を認めるが、異なる製品に含まれる異なる同位体の安全性の評価に要する根拠は不十分である。 |
| EC:欧州委員会 | サプリメントとしての最大量 | ・設定されていない (2004 年 5 月現在) |
|
| UK EVM: 英国ビタミン・ミネラル専門家委員会 |
上限安全摂取量(SUL)、サプリメントとして (LOAEL÷3) |
・7 mg/日 ・喫煙者は使用すべきでない |
20 mg と設定した LOAEL(最低副作用発現量)に慎重に選んだ不確実性係数 3 を適用し、成人における SUL として 7 mg をあてた。 |
| [文献 11,29 より引用改変] | |||
米国評議会(CRN USA)の見解は、12 年間にわたる健常男性への β-カロテン補給が悪性新生物や心血管疾患の発生率あるいは全死因死亡率に有益作用、有害作用のいずれももたらさなかった PHS の結果に基づいて 1 日 25 mg に相当する β-カロテンを 10 年以上にわたって摂取しても安全であることを示すデータがあるとして、非喫煙者に対する限定的な OSL として 25 mg/日という安全値を設けました。
同じ研究の結果でも、有益性を裏付ける証拠は認められなかった、あるいは影響をもたらさなかったという見方もあれば、同評議会のように特定の集団(ここでは非喫煙者)に対して安全とする見方もあるように、ATBC と CARET の結果に対する解釈も専門家間で一致をみることはまずないのではないでしょうか。
対象となった集団についてはその選定基準や食事摂取状況、β-カロテンについてはその投与開始時期、期間、量、他成分との組合せ方、あるいは喫煙によって発生するラジカルとの反応によってもたらされる酸化物質が及ぼす影響など、さまざまな原因がこれまでに考えられてきました。また、このような種類の介入試験を計画する際、参加者が非喫煙者あるいは過去喫煙者であっても考え得る危険性の回避のために β-カロテンを除外するケースも出てくるようになりました[23]。
「β-カロテンの供給源」、「体内分布」の項で述べたように β-カロテンは数多くの食品や私たちの体内で豊富な存在が認められるカロテノイドであるばかりでなく、「カロテン色素」、「カロテノイド色素」などとして広範囲にわたる加工食品の黄色系色素としての長い使用実績もあります。たとえサプリメントの利用機会がなくとも、さまざまな形態の食品から毎日のように私たちの体内に取り込んでいるカロテノイドの一つが β-カロテンです。それ故、ATBC や CARET で得られた結果は衝撃的でしたが、生理活性が高く、本来であれば健康利益が期待できるところの微量栄養素を単独あるいは限られた種類の組合せで高用量摂取することについて考え直すきっかけにもなったはずです。
このことは、β-カロテンに留まらず、人の健康に有益とされる他の抗酸化栄養素についても同様にいえることでしょう。例えば、米国で実施された VITAL コホート研究に参加した 50 歳から 76 歳までの男女 77,126 人からなる一般集団を対象とした研究で、β-カロテン、レチノールあるいはルテイン単一のサプリメントの長期使用に肺癌リスク上昇との有意な関連を認め、これらの成分の単独補給はとりわけ喫煙者の肺癌予防に推奨するべきではないという結論に達した研究は、その一部に過ぎません[30]。
カロテノイド研究は現在 β-カロテンを超えて、私たちの食事に見出される全ての色素について起っている事柄を理解する取り組みにまで広がりをみせており、そこから得られるさらなる知見に関心と期待が寄せられています。本サイトの開設目的はカロテノイドがもたらし得る健康利益について正確であるよう努めながら客観的な情報を提供することにあります。それ故、今回のような難しいテーマにおいてもそれが成し得たか内省し、更新の度に精度を高められるよう尽力してまいります。
最後に、ここでは限られた種類のリスクとの関係についてしか触れることができなかったことをお詫び申し上げます。心血管系の健康、メタボリックシンドローム、肝臓保護、認知機能、聴覚障害、加齢性眼疾患、皮膚の栄養と健康、骨・歯茎の健康、何種類かの癌、母子の健康と栄養など、他の分野につきましては以下のようなページで別途ご覧いただけます。
- 最近の研究から
- 文献データベース
- β-カロテンあるいはβ-カロテンと他の栄養成分との組み合わせが私たちの健康に果たす役割は、上述の分野以外でもさらに解明が進んでいます。関連情報は、疫学調査、臨床試験、あるいは in vitro、in vivo 実験の結果から得られた興味深い所見とともに、ライブラリーページで追加・更新しています。折に触れてご確認いただけましたら幸いです。
参考文献・参考URL
- 1.
-
- McCollum EV. The paths to the discovery of vitamins A and D. J Nutr. 1967 Feb;91(2):Suppl 1:11-6.
- 2.
-
- Symposium: Experiments That Changed Nutritional Thinking. J Nutr. 1997 May;127(5 Suppl):1017S-1053S.
- 3.
-
- Steenbock H. White corn vs. yellow corn and a probable relation between the fat-soluble vitamine and yellow plant pigments. Science. 1919 50:352-353.
- 4.
-
- Euler, Euler and Hellstrøm (1928). Biochem. Z. 203, 370.
- 5.
-
- "Richard Kuhn and the Chemical Institute: Double Bonds and Biological Mechanisms". Nobelprize.org. 15 Dec 2011
- http://www.nobelprize.org/nobel_prizes/medicine/articles/states/richard-kuhn.html (アクセス日:2011 年 12 月 15 日)
- 6.
-
- Online Etymology Dictionary http://www.etymonline.com/index.php?term=carotene (アクセス日:2011 年 12 月 19 日)
- 7.
-
- 文部科学省 科学技術・学術審議会・資源調査分科会 五訂増補日本食品標準成分表
- 8.
-
- 厚生労働省 「日本人の食事摂取基準」(2010 年版) http://www.mhlw.go.jp/shingi/2009/05/s0529-4.html (アクセス日: 2011 年 12 月 21 日)
- 9.
-
- 平成 21 年国民健康・栄養調査結果の概要 http://www.mhlw.go.jp/stf/houdou/2r9852000000xtwq.html (アクセス日:2011 年 12 月 21 日)
- 10.
-
- 平成 20 年国民健康・栄養調査結果の概要 http://www.mhlw.go.jp/houdou/2009/11/dl/h1109-1b.pdf (アクセス日:2011 年 12 月 21 日)
- 11.
-
- ジョン・ハズコック著、橋詰 直孝監訳、NNFA ジャパン(日本栄養・食品協会)訳(2007)『ビタミン・ミネラルの安全性(第 2 版)』第一出版
- 12.
-
- Khachik F, Nir Z, Ausich RL, Steck A, Pfander H. Distribution of carotenoids in fruits and vegetables as a criterion for the selection of appropriate chemopreventive agents. In: Yoshikawa T, Ohigashi H, eds. Food Factors for Cancer Prevention. Tokyo: Springer-Verlag; 1997. 204-8.
- 13.
-
- Khachik F, Carvalho L, Bernstein PS, Muir GJ, Zhao DY, Katz NB. Chemistry, distribution, and metabolism of tomato carotenoids and their impact on human health. Exp Biol Med (Maywood). 2002 Nov;227(10):845-51.
- 14.
-
- Khachik F, Spangler CJ, Smith JC Jr, Canfield LM, Steck A, Pfander H. Identification, quantification, and relative concentrations of carotenoids and their metabolites in human milk and serum. Anal Chem. 1997 May 15;69(10):1873-81.
- 15.
-
- Khachik F, Askin FB, Lai K. Distribution, bioavailability, and metabolism of carotenoids in humans. In: Bidlack WR, Omaye ST, Meskin MS, Jahner D. Eds. Phytochemicals, a New Paradigm. Lancaster, PA: Technomic Publishing; 1998. 77-96.
- 16.
-
- Hata TR, Scholz TA, Ermakov IV, McClane RW, Khachik F, Gellermann W, Pershing LK. Non-invasive Raman spectroscopic detection of carotenoids in human skin. J Invest Dermatol. 2000;115:441-8.
- 17.
-
- Gann PH, Khachik F. Tomatoes or lycopene versus prostate cancer: is evolution anti-reductionist? J Natl Cancer Inst. 2003 Nov 5;95(21):1563-5.
- 18.
-
- Bernstein PS, Khachik F, Carvalho LS, Muir GJ, Zhao DY, Katz NB. Identification and quantitation of carotenoids and their metabolites in the tissues of the human eye. Exp Eye Res. 2001 Mar;72(3):215-23.
- 19.
-
- Khachik F. Distribution and metabolism of dietary carotenoids in humans as a criterion for development of nutritional supplements. Pure Appl Chem. 2006; 78(8): 1551–7.
- 20.
-
- Seddon JM, Ajani UA, Sperduto RD, Hiller R, Blair N, Burton TC, Farber MD, Gragoudas ES, Haller J, Miller DT, Yannuzzi LA, Willett W. Dietary carotenoids, vitamin A, C, and E, and advanced age-related macular degeneration. JAMA. 1994;272:1413-20.
- 21.
-
- van Poppel G. Carotenoids and cancer: an update with emphasis on human intervention studies. Eur J Cancer. 1993;29A(9):1335-44.
- 22.
-
- Blot WJ, Li JY, Taylor PR, Guo W, Dawsey S, Wang GQ, Yang CS, Zheng SF, Gail M, Li GY, et al. Nutrition intervention trials in Linxian, China: supplementation with specific vitamin/mineral combinations, cancer incidence, and disease-specific mortality in the general population. J Natl Cancer Inst. 1993 Sep 15;85(18):1483-92.
- 23.
-
- Omenn GS. Interpretations of the Linxian Vitamin Supplement Chemoprevention Trials, Epidemiology. 1998 Jan;9(1):1-4.
- 24.
-
- The Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. N Engl J Med. 1994 Apr 14;330(15):1029-35.
- 25.
-
- Omenn GS, Goodman GE, Thornquist MD, Balmes J, Cullen MR, Glass A, Keogh JP, Meyskens FL Jr, Valanis B, Williams JH Jr, Barnhart S, Cherniack MG, Brodkin CA, Hammar S. Risk factors for lung cancer and for intervention effects in CARET, the Beta-Carotene and Retinol Efficacy Trial. J Natl Cancer Inst. 1996 Nov 6;88(21):1550-9.
- 26.
-
- Omenn GS, Goodman GE, Thornquist MD, Balmes J, Cullen MR, Glass A, Keogh JP, Meyskens FL, Valanis B, Williams JH, Barnhart S, Hammar S. Effects of a combination of beta carotene and vitamin A on lung cancer and cardiovascular disease. N Engl J Med. 1996 May 2;334(18):1150-5.
- 27.
-
- Hennekens CH, Buring JE, Manson JE, Stampfer M, Rosner B, Cook NR, Belanger C, LaMotte F, Gaziano JM, Ridker PM, Willett W, Peto R. Lack of effect of long-term supplementation with beta carotene on the incidence of malignant neoplasms and cardiovascular disease. N Engl J Med. 1996 May 2;334(18):1145-9.
- 28.
-
- European Commission Health & Consumer Protection Directorate-General – Scientific Committee on Food: Opinion of the scientific committee on food on the safety of β-carotene from all dietary sources. September 7 th 2000.
- 29.
-
- Hathcock JN. Vitamin and Mineral Safety 2 nd Edition. Council for Responsible Nutrition (CRN). 2004.
- 30.
-
- Satia JA, Littman A, Slatore CG, Galanko JA, White E. Long-term use of beta-carotene, retinol, lycopene, and lutein supplements and lung cancer risk: results from the VITamins And Lifestyle (VITAL) study. Am J Epidemiol. 2009 Apr 1;169(7):815-28.

